ในระหว่างปฏิกิริยา PCR มักพบปัจจัยรบกวนบางอย่างเกิดขึ้นได้
เนื่องจาก PCR มีความไวสูงมาก การปนเปื้อนจึงถือเป็นหนึ่งในปัจจัยสำคัญที่สุดที่ส่งผลต่อผลลัพธ์ของ PCR และอาจทำให้เกิดผลบวกปลอมได้
สิ่งที่สำคัญไม่แพ้กันคือแหล่งที่มาต่างๆ ที่นำไปสู่ผลลบเท็จ หากส่วนประกอบสำคัญอย่างน้อยหนึ่งส่วนของส่วนผสม PCR หรือปฏิกิริยาการขยายจำนวนถูกยับยั้งหรือรบกวน การทดสอบวินิจฉัยอาจได้รับผลกระทบ ซึ่งอาจนำไปสู่ประสิทธิภาพที่ลดลงและผลลบเท็จได้
นอกเหนือจากการยับยั้งแล้ว การสูญเสียความสมบูรณ์ของกรดนิวคลีอิกเป้าหมายอาจเกิดขึ้นได้เนื่องจากสภาวะการขนส่งและ/หรือการจัดเก็บก่อนการเตรียมตัวอย่าง โดยเฉพาะอย่างยิ่ง อุณหภูมิสูงหรือการจัดเก็บที่ไม่เหมาะสมอาจนำไปสู่ความเสียหายของเซลล์และกรดนิวคลีอิก การตรึงเซลล์และเนื้อเยื่อ และการฝังในพาราฟินเป็นสาเหตุที่ทราบกันดีของการแตกหักของ DNA และเป็นปัญหาที่เกิดขึ้นอย่างต่อเนื่อง (ดูรูปที่ 1 และ 2) ในกรณีเหล่านี้ แม้แต่การแยกและการทำให้บริสุทธิ์อย่างเหมาะสมก็จะไม่ช่วยอะไร
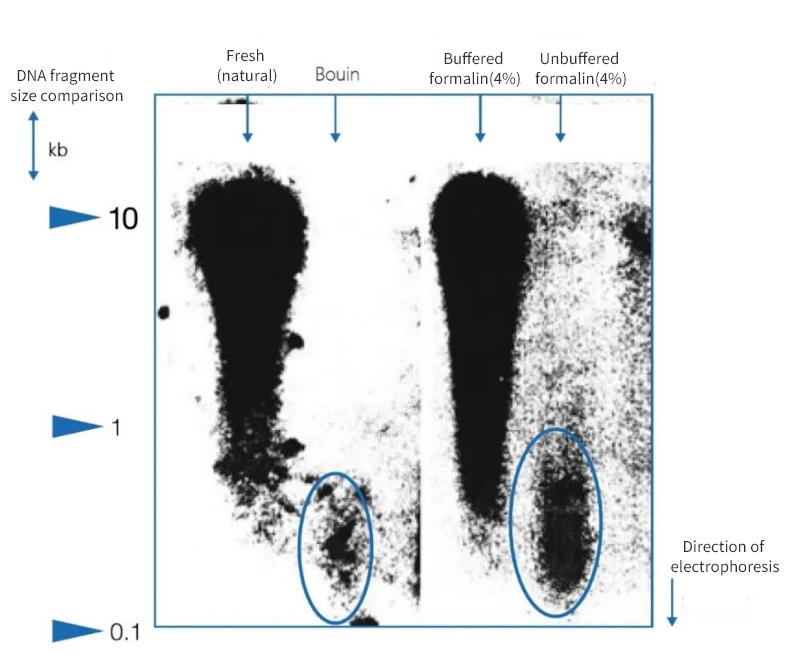
รูปที่ 1 | ผลกระทบของการตรึงต่อความสมบูรณ์ของดีเอ็นเอ
การวิเคราะห์ด้วยเจลอิเล็กโทรโฟเรซิสแบบอะกาโรสแสดงให้เห็นว่าคุณภาพของดีเอ็นเอที่แยกได้จากชิ้นเนื้อพาราฟินจากการชันสูตรศพมีความแตกต่างกันอย่างมาก ดีเอ็นเอที่มีความยาวเฉลี่ยของชิ้นส่วนแตกต่างกันนั้นพบได้ในสารสกัดขึ้นอยู่กับวิธีการตรึง ดีเอ็นเอจะได้รับการรักษาไว้เฉพาะเมื่อตรึงในตัวอย่างแช่แข็งตามธรรมชาติและในฟอร์มาลินที่เป็นกลางที่มีบัฟเฟอร์เท่านั้น การใช้สารตรึง Bouin ที่เป็นกรดเข้มข้นหรือฟอร์มาลินที่ไม่มีบัฟเฟอร์และมีกรดฟอร์มิกส่งผลให้ดีเอ็นเอสูญหายไปอย่างมาก ส่วนที่เหลืออยู่นั้นแตกหักเป็นชิ้นส่วนเล็กๆ จำนวนมาก
ทางด้านซ้าย ความยาวของชิ้นส่วนจะแสดงเป็นกิโลเบสคู่ (kbp)
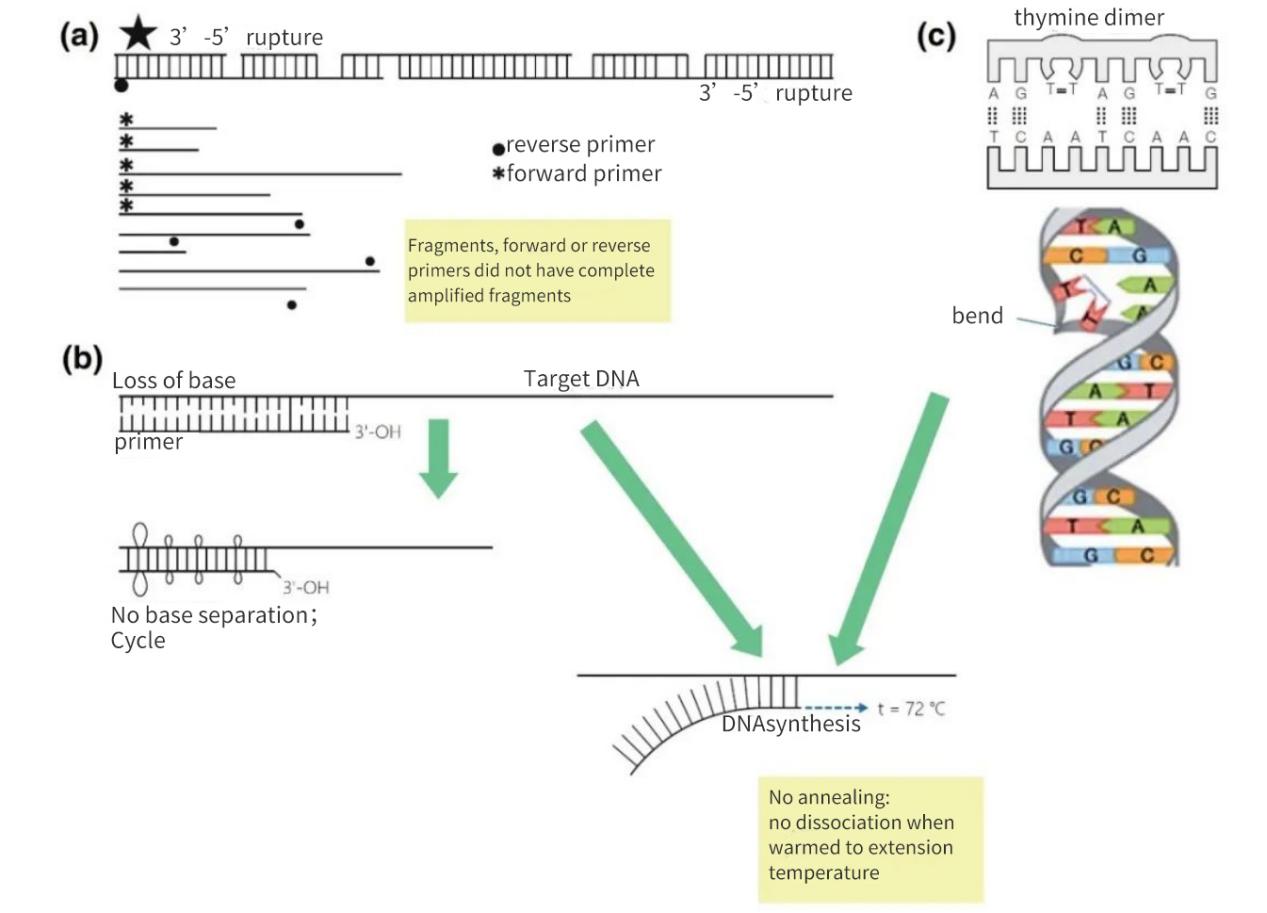
รูปที่ 2 | การสูญเสียความสมบูรณ์ของเป้าหมายกรดนิวคลีอิก
(a) ช่องว่าง 3′-5′ บนสายทั้งสองจะส่งผลให้เกิดการแตกหักในดีเอ็นเอเป้าหมาย การสังเคราะห์ดีเอ็นเอจะยังคงเกิดขึ้นบนชิ้นส่วนเล็กๆ นั้น อย่างไรก็ตาม หากไม่มีตำแหน่งการจับคู่ของไพรเมอร์บนชิ้นส่วนดีเอ็นเอ การขยายตัวแบบเชิงเส้นเท่านั้นที่จะเกิดขึ้น ในกรณีที่ดีที่สุด ชิ้นส่วนอาจอิ่มตัวซึ่งกันและกัน แต่ผลผลิตจะน้อยและต่ำกว่าระดับการตรวจจับ
(b) การสูญเสียเบส ซึ่งส่วนใหญ่เกิดจากการดีพิวริเนชันและการก่อตัวของไทมิดีนไดเมอร์ ส่งผลให้จำนวนพันธะไฮโดรเจนลดลงและค่า Tm ลดลง ในระหว่างช่วงการให้ความร้อนที่ยาวนาน ไพรเมอร์จะแยกตัวออกจากเมทริกซ์ DNA และจะไม่เกิดการจับคู่กันแม้ในสภาวะที่ไม่เข้มงวดมากนัก
(c) เบสไทมีนที่อยู่ติดกันจะก่อตัวเป็นไดเมอร์ TT
อีกปัญหาหนึ่งที่มักเกิดขึ้นในการวินิจฉัยระดับโมเลกุลคือ การปลดปล่อยกรดนิวคลีอิกเป้าหมายที่ไม่เหมาะสมเมื่อเทียบกับการสกัดด้วยฟีนอล-คลอโรฟอร์ม ในกรณีที่รุนแรง อาจส่งผลให้เกิดผลลบเท็จได้ การสลายเซลล์ด้วยการต้มหรือการย่อยเศษเซลล์ด้วยเอนไซม์สามารถช่วยประหยัดเวลาได้มาก แต่โดยทั่วไปแล้ววิธีนี้มักส่งผลให้ความไวของ PCR ต่ำเนื่องจากการปลดปล่อยกรดนิวคลีอิกไม่เพียงพอ
การยับยั้งการทำงานของพอลิเมอเรสระหว่างการขยายจำนวน
โดยทั่วไป คำว่า "การยับยั้ง" ถูกใช้เป็นแนวคิดหลักเพื่ออธิบายปัจจัยทั้งหมดที่นำไปสู่ผลลัพธ์ PCR ที่ไม่เหมาะสม ในแง่ชีวเคมีอย่างเคร่งครัด การยับยั้งจะจำกัดอยู่เฉพาะกิจกรรมของเอนไซม์ กล่าวคือ มันจะลดหรือป้องกันการเปลี่ยนสารตั้งต้นเป็นผลิตภัณฑ์ผ่านการโต้ตอบกับบริเวณออกฤทธิ์ของเอนไซม์ DNA polymerase หรือโคแฟคเตอร์ของมัน (เช่น Mg2+ สำหรับ Taq DNA polymerase)
ส่วนประกอบในตัวอย่างหรือบัฟเฟอร์และสารสกัดต่างๆ ที่มีสารเคมี อาจยับยั้งเอนไซม์โดยตรงหรือดักจับโคแฟคเตอร์ของเอนไซม์ (เช่น EDTA) ซึ่งจะทำให้พอลิเมอเรสไม่ทำงาน และส่งผลให้ผลการตรวจ PCR ลดลงหรือได้ผลลบเท็จ
อย่างไรก็ตาม ปฏิกิริยาระหว่างส่วนประกอบของปฏิกิริยาและกรดนิวคลีอิกที่มีเป้าหมายอยู่จำนวนมากก็ถูกกำหนดให้เป็น 'สารยับยั้ง PCR' ด้วยเช่นกัน เมื่อความสมบูรณ์ของเซลล์ถูกทำลายโดยกระบวนการแยกและกรดนิวคลีอิกถูกปล่อยออกมา ปฏิกิริยาระหว่างตัวอย่างและสารละลายและเฟสของแข็งโดยรอบอาจเกิดขึ้นได้ ตัวอย่างเช่น 'สารดักจับ' สามารถจับกับ DNA สายเดี่ยวหรือสายคู่ผ่านปฏิกิริยาที่ไม่ใช่พันธะโควาเลนต์ และรบกวนกระบวนการแยกและทำให้บริสุทธิ์โดยการลดจำนวนเป้าหมายที่ไปถึงภาชนะปฏิกิริยา PCR ในที่สุด
โดยทั่วไป สารยับยั้ง PCR พบได้ในของเหลวในร่างกายส่วนใหญ่ และในสารเคมีที่ใช้ในการตรวจวินิจฉัยทางคลินิก (ยูเรียในปัสสาวะ ฮีโมโกลบินและเฮปารินในเลือด) ผลิตภัณฑ์เสริมอาหาร (ส่วนประกอบอินทรีย์ ไกลโคเจน ไขมัน ไอออน Ca2+) และส่วนประกอบในสิ่งแวดล้อม (ฟีนอล โลหะหนัก)
| สารยับยั้ง | แหล่งที่มา |
| ไอออนแคลเซียม | นม เนื้อเยื่อกระดูก |
| คอลลาเจน | เนื้อเยื่อ |
| เกลือน้ำดี | อุจจาระ |
| เฮโมโกลบิน | ในเลือด |
| เฮโมโกลบิน | ตัวอย่างเลือด |
| กรดฮิวมิก | ดิน, พืช |
| เลือด | เลือด |
| แลคโตเฟอร์ริน | เลือด |
| เมลานิน (ยุโรป) | ผิวหนัง, เส้นผม |
| ไมโอโกลบิน | เนื้อเยื่อกล้ามเนื้อ |
| โพลีแซ็กคาไรด์ | พืช, มูลสัตว์ |
| โปรตีเอส | น้ำนม |
| ยูเรีย | ปัสสาวะ |
| มิวโคโพลีแซคคาไรด์ | กระดูกอ่อน, เยื่อเมือก |
| ลิกนิน เซลลูโลส | พืช |
สารยับยั้ง PCR ที่พบได้ทั่วไปมักพบในแบคทีเรียและเซลล์ยูคาริโอต ดีเอ็นเอที่ไม่ใช่เป้าหมาย โมเลกุลขนาดใหญ่ที่จับกับดีเอ็นเอในเมทริกซ์ของเนื้อเยื่อ และอุปกรณ์ในห้องปฏิบัติการ เช่น ถุงมือและพลาสติก การทำให้กรดนิวคลีอิกบริสุทธิ์ระหว่างหรือหลังการสกัดเป็นวิธีที่เหมาะสมที่สุดในการกำจัดสารยับยั้ง PCR
ปัจจุบัน อุปกรณ์สกัดอัตโนมัติต่างๆ สามารถทดแทนกระบวนการแบบใช้มือได้หลายอย่าง แต่ยังไม่เคยมีการกู้คืนและ/หรือทำให้บริสุทธิ์เป้าหมายได้ 100% สารยับยั้งที่มีศักยภาพอาจยังคงอยู่ในกรดนิวคลีอิกที่บริสุทธิ์แล้ว หรืออาจออกฤทธิ์ไปแล้ว มีกลยุทธ์ต่างๆ เพื่อลดผลกระทบของสารยับยั้ง การเลือกใช้พอลิเมอเรสที่เหมาะสมสามารถส่งผลกระทบอย่างมากต่อกิจกรรมของสารยับยั้ง วิธีการอื่นๆ ที่ได้รับการพิสูจน์แล้วว่าช่วยลดการยับยั้ง PCR ได้แก่ การเพิ่มความเข้มข้นของพอลิเมอเรส หรือการเติมสารเติมแต่ง เช่น BSA
การยับยั้งปฏิกิริยา PCR สามารถแสดงให้เห็นได้โดยการใช้การควบคุมคุณภาพกระบวนการภายใน (IPC)
ต้องระมัดระวังเป็นอย่างยิ่งในการกำจัดสารเคมีและสารละลายอื่นๆ ทั้งหมดในชุดสกัด เช่น เอทานอล, EDTA, CETAB, LiCl, GuSCN, SDS, ไอโซโพรพานอล และฟีนอล ออกจากสารพันธุกรรมที่แยกได้ โดยต้องล้างให้สะอาดหมดจด เนื่องจากความเข้มข้นของสารเหล่านี้อาจกระตุ้นหรือยับยั้งปฏิกิริยา PCR ได้
วันที่เผยแพร่: 19 พฤษภาคม 2023
 中文网站
中文网站